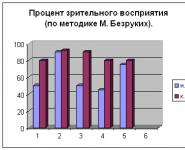
Термин коррозия. Виды коррозии
Химическая коррозия - это процесс, состоящий в разрушении металла при взаимодействии с агрессивной внешней средой. Химическая разновидность коррозийных процессов не имеет связи с воздействием электрического тока. При этом виде коррозии происходит окислительная реакция, где разрушаемый материал - одновременно восстановитель элементов среды.

Классификация разновидности агрессивной среды включает два вида разрушения металла:
- химическая коррозия в жидкостях-неэлектролитах;
- химическая газовая коррозия.
Газовая коррозия
Самая частая разновидность химической коррозии - газовая - представляет собой коррозийный процесс, происходящий в газах при повышенных температурах. Указанная проблема характерна для работы многих типов технологического оборудования и деталей (арматуры печей, двигателей, турбин и т.д.). Кроме того, сверхвысокие температуры используются при обработке металлов под высоким давлением (нагревание перед прокаткой, штамповкой, ковкой, термическими процессами и т.д.).
Особенности состояния металлов при повышенных температурах обуславливаются двумя их свойствами - жаропрочностью и жаростойкостью. Жаропрочность - это степень устойчивости механических свойств металла при сверхвысоких температурах. Под устойчивостью механических свойств понимается сохранение прочности в течение продолжительного времени и сопротивляемость ползучести. Жаростойкость - это устойчивость металла к коррозионной активности газов в условиях повышенных температур.

Скорость развития газовой коррозии обуславливается рядом показателей, в числе которых:
- температура атмосферы;
- компоненты, входящие в металл или сплав;
- параметры среды, где находятся газы;
- продолжительность контактирования с газовой средой;
- свойства коррозийных продуктов.
На коррозийный процесс больше влияние оказывают свойства и параметры оксидной пленки, появившейся на металлической поверхности. Образование окисла можно хронологически разделить на два этапа:
- адсорбция кислородных молекул на металлической поверхности, взаимодействующей с атмосферой;
- контактирование металлической поверхности с газом, в результате чего возникает химическое соединение.

Первый этап характеризуется появлением ионной связи, как следствие взаимодействия кислорода и поверхностных атомов, когда кислородный атом отбирает пару электроном у металла. Возникшая связь отличается исключительной силой - она больше, нежели связь кислорода с металлом в окисле.
Объяснение такой связи кроется в действии атомного поля на кислород. Как только поверхность металла наполняется окислителем (а это происходит очень быстро), в условиях низких температур, благодаря силе Ван-дер-Ваальса, начинается адсорбция окислительных молекул. Результат реакции - возникновение тончайшей мономолекулярной пленки, которая с течением времени становится толще, что усложняет доступ кислорода.
На втором этапе происходит химическая реакция, в ходе которой окислительный элемент среды отбирает у металла валентные электроны. Химическая коррозия - конечный результат реакции.
Характеристики оксидной пленки
Классификация оксидных пленок включает их три разновидности:
- тонкие (незаметны без специальных приборов);
- средние (цвета побежалости);
- толстые (видны невооруженным взглядом).
Появившаяся оксидная пленка имеет защитные возможности - она замедляет или даже полностью угнетает развитие химической коррозии. Также наличие оксидной пленки повышает жаростойкость металла.
Однако, действительно эффективная пленка должна отвечать ряду характеристик:
- быть не пористой;
- иметь сплошную структуру;
- обладать хорошими адгезивными свойствами;
- отличаться химической инертностью в отношении с атмосферой;
- быть твердой и устойчивой к износу.
Одно из указанных выше условий - сплошная структура имеет особенно важное значение. Условие сплошности - превышение объема молекул оксидной пленки над объемом атомов металла. Сплошность - это возможность окисла накрыть сплошным слоем всю металлическую поверхность. При несоблюдении этого условия, пленка не может считаться защитной. Однако, из этого правила имеются исключения: для некоторых металлов, например, для магния и элементов щелочно-земельной групп (исключая бериллий), сплошность не относится к критически важным показателям.

Чтобы установить толщину оксидной пленки, используются несколько методик. Защитные качества пленки можно выяснить в момент ее образования. Для этого изучаются скорость окисления металла, и параметры изменения скорости во времени.
Для уже сформированного окисла применяется другой метод, состоящий в исследовании толщины и защитных характеристик пленки. Для этого на поверхность накладывается реагент. Далее специалисты фиксируют время, которое понадобится на проникновение реагента, и на основании полученных данных делают вывод о толщине пленки.
Обратите внимание! Даже окончательно сформировавшаяся оксидная пленка продолжает взаимодействовать с окислительной средой и металлом.
Скорость развития коррозии
Интенсивность, с какой развивается химическая коррозия, зависит от температурного режима. При высокой температуре окислительные процессы развиваются стремительнее. Причем снижение роли термодинамического фактора протекания реакции не влияет на процесс.
Немалое значение имеет охлаждение и переменный нагрев. Из-за термических напряжений в оксидной пленке появляются трещины. Через прорехи окислительный элемент попадает на поверхность. В результате образуется новый слой оксидной пленки, а прежний - отслаивается.

Не последнюю роль играют и компоненты газовой среды. Этот фактор индивидуален для разных видов металлов и согласуется с температурными колебаниями. К примеру, медь быстро поддается коррозии, если она контактирует с кислородом, но отличается устойчивостью к этому процессу в среде оксида серы. Для никеля же напротив, серный оксид губителен, а устойчивость наблюдается в кислороде, диоксиде углерода и водной среде. А вот хром проявляет стойкость ко всем перечисленным средам.
Обратите внимание! Если уровень давления диссоциации окисла превышает давление окисляющего элемента, окислительный процесс останавливается и металл обретает термодинамическую устойчивость.
На скорость окислительной реакции влияют и компоненты сплава. Например, марганец, сера, никель и фосфор никак не способствуют окислению железа. А вот алюминий, кремний и хром делают процесс более медленным. Еще сильнее замедляют окисление железа кобальт, медь, бериллий и титан. Сделать процесс более интенсивным помогут добавки ванадия, вольфрама и молибдена, что объясняется легкоплавкостью и летучестью данных металлов. Наиболее медленно окислительные реакции протекают при аустенитной структуре, поскольку она наиболее приспособлена к высоким температурам.

Еще один фактор, от которого зависит скорость коррозии, - характеристика обработанной поверхности. Гладкая поверхность окисляется медленнее, а неровная - быстрее.
Коррозия в жидкостях-неэлектролитах
К неэлектропроводным жидким средам (т.е. жидкостям-неэлектролитам) относят такие органические вещества, как:
- бензол;
- хлороформ;
- спирты;
- тетрахлорид углерода;
- фенол;
- нефть;
- бензин;
- керосин и т.д.

Кроме того, к жидкостям-неэлектролитам причисляют небольшое количество неорганических жидкостей, таких как жидкий бром и расплавленная сера.
При этом нужно заметить, что органические растворители сами по себе не вступают в реакцию с металлами, однако, при наличии небольшого объема примесей возникает интенсивный процесс взаимодействия.
Увеличивают скорость коррозии находящиеся в нефти серосодержащие элементы. Также, усиливают коррозийные процессы высокие температуры и присутствие в жидкости кислорода. Влага интенсифицирует развитие коррозии в соответствии с электромеханическим принципом.
Еще один фактор быстрого развития коррозии - жидкий бром. При нормальных температурах он особенно разрушительно воздействует на высокоуглеродистые стали, алюминий и титан. Менее существенно влияние брома на железо и никель. Самую большую устойчивость к жидкому брому показывают свинец, серебро, тантал и платина.

Расплавленная сера вступает в агрессивную реакцию почти со всеми металлами, в первую очередь со свинцом, оловом и медью. На углеродистые марки стали и титан сера влияет меньше и почти совсем разрушает алюминий.
Защитные мероприятия для металлоконструкций, находящихся в неэлектропроводных жидких средах, проводят добавлением устойчивым к конкретной среде металлов (например, сталей с высоким содержанием хрома). Также, применяются особые защитные покрытия (например, в среде, где содержится много серы, используют алюминиевые покрытия).
Способы защиты от коррозии
Методы борьбы с коррозией включают:

Выбор конкретного материала зависит от потенциальной эффективности (в том числе технологической и финансовой) его использования.
Современные принципы защиты металла основываются на таких методиках:
- Улучшение химической сопротивляемости материалов. Успешно зарекомендовали себя химически стойкие материалы (высокополимерные пластики, стекло, керамика).
- Изолирование материала от агрессивной среды.
- Уменьшение агрессивности технологической среды. В качестве примеров таких действий можно привести нейтрализацию и удаление кислотности в коррозийных средах, а также использование всевозможных ингибиторов.
- Электрохимическая защита (наложение внешнего тока).
Указанные выше методики подразделяются на две группы:
- Повышение химической сопротивляемости и изолирование применяются до того, как металлоконструкция запускается в эксплуатацию.
- Уменьшение агрессивности среды и электрохимическая защита используются уже в процессе применения изделия из металла. Применение этих двух методик дает возможность внедрять новые способы защиты, в результате которых защита обеспечивается изменением эксплуатационных условий.
Один из самых часто применяемых способов защиты металла - гальваническое антикоррозийное покрытие - экономически нерентабелен при значительных площадях поверхностей. Причина в высоких затратах на подготовительный процесс.

Ведущее место среди способов защиты занимает покрытие металлов лакокрасочными материалами. Популярность такого метода борьбы с коррозией обусловлена совокупностью нескольких факторов:
- высокие защитные свойства (гидрофобность, отталкивание жидкостей, невысокие газопроницаемость и паропроницаемость);
- технологичность;
- широкие возможности для декоративных решений;
- ремонтопригодность;
- экономическая оправданность.
В то же время, использование широкодоступных материалов не лишено недостатков:
- неполное увлажнение металлической поверхности;
- нарушенное сцепление покрытия с основным металлом, что ведет к скапливанию электролита под антикоррозийным покрытием и, таким образом, способствует коррозии;
- пористость, приводящая к повышенной влагопроницаемости.
И все же, окрашенная поверхность защищает металл от коррозийных процессов даже при фрагментарном повреждении пленки, тогда как несовершенные гальванические покрытия способны даже ускорять коррозию.
Органосиликатные покрытия

Химическая коррозия практически не распространяется на органосиликатные материалы. Причины этого кроются в повышенной химической устойчивости таких композиций, их стойкости к свету, гидрофобных качествах и невысоком водопоглощении. Также органосиликаты устойчивы к низким температурам, обладают хорошими адгезивными свойствами и износостойкостью.
Проблемы разрушения металлов из-за воздействия коррозии не исчезают, несмотря на развитие технологий борьбы с ними. Причина в постоянном возрастании объемов производства металлов и все более сложных условий эксплуатации изделий из них. Окончательно решить проблему на данном этапе нельзя, поэтому усилия ученых сосредоточены на поисках возможностей по замедлению коррозионных процессов.
КОРРОЗИЯ МЕТАЛЛОВ – физико-химическое или химическое взаимодействие между металлом (сплавом) и средой, приводящее к ухудшению функциональных свойств металла (сплава), среды или включающей их технической системы.
Слово коррозия происходит от латинского «corrodo» – «грызу» (позднелатинское «corrosio» означает «разъедание»).
Коррозия вызывается химической реакцией металла с веществами окружающей среды, протекающей на границе металла и среды. Чаще всего это окисление металла, например, кислородом воздуха или кислотами, содержащимися в растворах, с которыми контактирует металл. Особенно подвержены этому металлы, расположенные в ряду напряжений (ряду активности) левее водорода , в том числе железо .
В результате коррозии железо ржавеет. Этот процесс очень сложен и включает несколько стадий. Его можно описать суммарным уравнением:
4Fe + 6H 2 O (влага) + 3O 2 (воздух) = 4Fe(OH) 3
Гидроксид железа(III) очень неустойчив, быстро теряет воду и превращается в оксид железа(III). Это соединение не защищает поверхность железа от дальнейшего окисления. В результате железный предмет может быть полностью разрушен.
Многие металлы, в том числе и довольно активные (например, алюминий) при коррозии покрываются плотной, хорошо скрепленной с металлами оксидной пленкой, которая не позволяет окислителям проникнуть в более глубокие слои и потому предохраняет металл от коррозии. При удалении этой пленки металл начинает взаимодействовать с влагой и кислородом воздуха.
Алюминий в обычных условиях устойчив к воздействию воздуха и воды, даже кипящей, однако если на поверхность алюминия нанести ртуть, то образующаяся амальгама разрушает оксидную пленку – выталкивает ее с поверхности, и металл быстро превращается в белые хлопья метагидроксида алюминия:
4Al + 2H 2 O + 3O 2 = 4AlO(OH)
Амальгамированный алюминий взаимодействует с водой с выделением водорода:
2Al + 4H 2 O = 2AlO(OH) + 3H 2
Коррозии подвергаются и некоторые довольно мало активные металлы. Во влажном воздухе поверхность меди покрывается зеленоватым налетом (патиной) в результате образования смеси основных солей.
Иногда при коррозии металлов происходит не окисление, а восстановление некоторых элементов, содержащихся в сплавах. Например, при высоких давлениях и температурах карбиды, содержащиеся в сталях, восстанавливаются водородом.
Разрушение металлов в присутствии водорода обнаружили в середине девятнадцатого века. Французский инженер Сент Клэр Девиль изучал причины неожиданных разрывов орудийных стволов. При их химическом анализе он нашел в металле водород. Девиль решил, что именно водородное насыщение явилось причиной внезапного падения прочности стали.
Много хлопот доставил водород конструкторам оборудования для одного из важнейших промышленных химических процессов – синтеза аммиака. Первые аппараты для этого синтеза служили лишь десятки часов, а затем разлетались на мелкие части. Только добавление в сталь титана, ванадия или молибдена помогло решить эту проблему.
К коррозии металлов можно отнести также их растворение в жидких расплавленных металлах (натрий, свинец, висмут), которые используются, в частности, в качестве теплоносителей в ядерных реакторах.
По стехиометрии реакции, описывающие коррозию металлов, довольно просты, однако по механизму они относятся к сложным гетерогенным процессам. Механизм коррозии определяется, прежде всего, типом агрессивной среды.
При контакте металлического материала с химически активным газом на его поверхности появляется пленка продуктов реакции. Она препятствует дальнейшему контакту металла и газа. Если сквозь эту пленку происходит встречная диффузия реагирующих веществ, то реакция продолжается. Процесс облегчается при высоких температурах. В ходе коррозии пленка продукта непрерывно утолщается, а металл разрушается. Большие убытки от газовой коррозии терпит металлургия и другие отрасли промышленности, где используются высокие температуры.
Наиболее распространена коррозия в средах электролитов. В некоторых технологических процессах металлы контактируют с расплавами электролитов. Однако чаще всего коррозия протекает в растворах электролитов. Металл не обязательно должен быть полностью погружен в жидкость. Растворы электролитов могут находиться в виде тонкой пленки на поверхности металла. Они нередко пропитывают окружающую металл среду (почву, бетон и др.).
Во время строительства метромоста и станции «Ленинские горы» в Москве в бетон добавляли большое количество хлорида натрия, чтобы не допустить замерзания еще не схватившегося бетона. Станция была сооружена в кратчайшие сроки (всего за 15 месяцев) и открыта 12 января 1959. Однако присутствие хлорида натрия в бетоне вызвало разрушение стальной арматуры. Коррозии оказались подвергнуты 60% железобетонных конструкций, поэтому станция была закрыта на реконструкцию, продолжавшуюся почти 10 лет. Лишь 14 января 2002 состоялось повторное открытие метромоста и станции, получившей название «Воробьевы горы».
Использование солей (обычно хлорида натрия или кальция) для удаления снега и льда с дорог и тротуаров также приводит к ускоренному разрушению металлов. Сильно страдают транспортные средства и подземные коммуникации. Подсчитано, что только в США применение солей для борьбы со снегопадами и гололедом приводит к потерям на сумму около 2 млрд. долл. в год в связи с коррозией двигателей и 0,5 млрд. долл. на дополнительный ремонт дорог, подземных магистралей и мостов.
В средах электролитов коррозия обусловлена не только действием кислорода, воды или кислот на металлы, но и электрохимическими процессами. Уже в начале 19 в. электрохимическую коррозию изучали английские ученые Гемфри Дэви и Майкл Фарадей. Первая теория электрохимической коррозии была выдвинута в 1830 швейцарским ученым Де ла Ривом. Она объясняла возникновение коррозии в месте контакта двух разных металлов.
Электрохимическая коррозия приводит к быстрому разрушению более активных металлов, которые в различных механизмах и устройствах контактируют с менее активными металлами, расположенными в электрохимическом ряду напряжений правее. Использование медных или латунных деталей в железных или алюминиевых конструкциях, которые работают в морской воде, существенно усиливает коррозию. Известны случаи разрушения и затопления кораблей, железная обшивка которых была скреплена медными заклепками.
По отдельности алюминий и титан устойчивы к действию морской воды, но если они контактируют в одном изделии, например в боксе для подводной фототехники, алюминий очень быстро разрушается, и бокс протекает.
Электрохимические процессы могут протекать и в однородном металле. Они активизируются, если есть различия в составе зерна металла в объеме и на границе, неоднородное механическое напряжение, микропримеси и т.д. В разработке общей теории электрохимической коррозии металлических материалов участвовали многие наши соотечественники, в том числе Владимир Александрович Кистяковский (1865–1952) и Александр Наумович Фрумкин (1895–1976).
Одной из причин возникновения электрохимической коррозии являются блуждающие токи, которые появляются вследствие утечки части тока из электрических цепей в почву или водные растворы, где они попадают на металлические конструкции. В местах выхода тока из этих конструкций вновь в почву или воду начинается растворение металла. Такие зоны разрушения металлов под действием блуждающих токов особенно часто наблюдаются в районах наземного электрического транспорта (трамвайные линии, железнодорожный транспорт на электрической тяге). Эти токи могут достигать несколько ампер, что приводит к большим коррозионным разрушениям. Например, прохождение тока силой в 1 А в течение одного года вызовет растворение 9,1 кг железа, 10,7 кг цинка, 33,4 кг свинца.
Коррозия может возникать и под влиянием радиационного излучения, а также продуктов жизнедеятельности бактерий и других организмов. С развитием бактерий на поверхности металлических конструкций связано явление биокоррозии. Обрастание подводной части судов мелкими морскими организмами также оказывает влияние на коррозионные процессы.
При одновременном воздействии на металл внешней среды и механических напряжений все коррозионные процессы активизируются, поскольку при этом понижается термическая устойчивость металла, нарушаются оксидные пленки на поверхности металла, усиливаются электрохимические процессы в местах появления трещин и неоднородностей.
Коррозия приводит к огромным безвозвратным потерям металлов, ежегодно полностью разрушается около 10% производимого железа. По данным Института физической химии РАН, каждая шестая домна в России работает впустую – весь выплавляемый металл превращается в ржавчину. Разрушение металлических конструкций, сельскохозяйственных и транспортных машин, промышленной аппаратуры становится причиной простоев, аварий, ухудшения качества продукции. Учет возможной коррозии приводит к повышенным затратам металла при изготовлении аппаратов высокого давления, паровых котлов, металлических контейнеров для токсичных и радиоактивных веществ и т.д. Это увеличивает общие убытки от коррозии. Немалые средства приходится тратить на противокоррозионную защиту. Соотношение прямых убытков, косвенных убытков и расходов на защиту от коррозии оценивают как (3–4):1:1. В промышленно развитых странах ущерб от коррозии достигает 4% национального дохода. В нашей стране он исчисляется миллиардами рублей в год.
Проблемы коррозии постоянно обостряются из-за непрерывного роста производства металлов и ужесточения условий их эксплуатации. Среда, в которой используются металлические конструкции, становится все более агрессивной, в том числе и за счет ее загрязнения. Металлические изделия, используемые в технике, работают в условиях все более высоких температур и давлений, мощных потоков газов и жидкостей. Поэтому вопросы защиты металлических материалов от коррозии становятся все более актуальными. Полностью предотвратить коррозию металлов невозможно, поэтому единственным путем борьбы с ней является поиск способов ее замедления.
Проблема защиты металлов от коррозии возникла почти в самом начале их использования. Люди пытались защитить металлы от атмосферного воздействия с помощью жира, масел, а позднее и покрытием другими металлами и, прежде всего, легкоплавким оловом (лужением). В трудах древнегреческого историка Геродота (5 в. до н. э.) и древнеримского ученого Плиния Старшего (1 в. до н. э.) уже есть упоминания о применении олова для предохранения железа от ржавления. В настоящее время борьбу с коррозией ведут сразу в нескольких направлениях – пытаются изменить среду, в которой работает металлическое изделие, повлиять на коррозионную устойчивость самого материала, предотвратить контакт между металлом и агрессивными веществами внешней среды.
Полностью предотвратить коррозию можно только в инертной среде, например в атмосфере аргона, однако реально создать такую среду при эксплуатации конструкций и механизмов в подавляющем большинстве случаев невозможно. На практике для снижения коррозионной активности среды из нее стараются удалить наиболее реакционноспособные компоненты, например, снижают кислотность водных растворов и почв, с которыми могут контактировать металлы. Одним из методов борьбы с коррозией железа и его сплавов, меди, латуни, цинка, свинца является удаление из водных растворов кислорода и диоксида углерода. В энергетике и некоторых отраслях техники воду освобождают также от хлоридов, которые стимулируют локальную коррозию. Для снижения кислотности почвы проводят известкование.
Агрессивность атмосферы сильно зависит от влажности. Для любого металла есть некоторая критическая относительная влажность, ниже которой он не подвергается атмосферной коррозии. Для железа, меди, никеля, цинка она составляет 50–70%. Иногда для сохранности изделий, имеющих историческую ценность, их температуру искусственно поддерживают выше точки росы. В закрытых пространствах (например, в упаковочных коробках) влажность понижают с помощью силикагеля или других адсорбентов. Агрессивность промышленной атмосферы определяется, в основном продуктами сгорания топлива (см . ЗАГРЯЗНЕНИЕ ОКРУЖАЮЩЕЙ СРЕДЫ). Уменьшению потерь от коррозии способствует предотвращение кислотных дождей и устранение вредных газовых выбросов.
Разрушение металлов в водных средах можно замедлить при помощи ингибиторов коррозии, которые в небольших количествах (обычно менее 1%) вводят в водные растворы. Они способствуют пассивированию поверхности металла, то есть образованию тонкой и плотной пленки оксидов или других малорастворимых соединений, которая препятствует разрушению основного вещества. Для этой цели применяют некоторые соли натрия (карбонат, силикат, борат) и другие соединения. Если бритвенные лезвия погрузить в раствор хромата калия, они хранятся намного дольше. Часто используют органические ингибиторы, которые более эффективны, чем неорганические.
Один из способов защиты от коррозии основывается на разработке новых материалов, обладающих более высокой коррозионной стойкостью. Постоянно ведутся поиски заменителей коррозирующих металлов. Пластмассы, керамика, стекло, резина, асбест и бетон более устойчивы к воздействию окружающей среды, однако по многим другим свойствам они уступают металлам, которые по-прежнему служат основными конструкционными материалами.
Благородные металлы практически не поддаются коррозии, но для широкого применения они слишком дороги, поэтому их используют лишь в наиболее ответственных деталях, например для изготовления некорродирующих электрических контактов. Высокой коррозионной стойкостью обладают никель, алюминий, медь, титан и сплавы на их основе. Их производство растет довольно быстро, однако и сейчас наиболее доступным и широко используемым металлом остается быстро ржавеющее железо. Для придания коррозионной стойкости сплавам на основе железа часто используют легирование. Так получают нержавеющую сталь, которая, помимо железа, содержит хром и никель. Самая распространенная в наше время нержавеющая сталь марки 18–8 (18% хрома и 8% никеля) появилась в 1923. Она вполне устойчива к воздействию влаги и кислорода. Первые тонны нержавеющей стали в нашей стране были выплавлены в 1924 в Златоусте. Сейчас разработано много марок таких сталей, которые, помимо хрома и никеля, содержат марганец, молибден, вольфрам и другие химические элементы. Часто применяют поверхностное легирование недорогих железных сплавов цинком, алюминием, хромом.
Для противостояния атмосферной коррозии на стальные изделия наносятся тонкие покрытия из других металлов, более устойчивых к воздействию влаги и кислорода воздуха. Часто используются покрытия из хрома и никеля. Поскольку хромовые покрытия нередко содержат трещины, их обычно наносят поверх менее декоративных никелевых покрытий. На защиту жестяных консервных банок от коррозии в органических кислотах, содержащихся в пищевых продуктах, расходуется значительное количество олова. Долгое время для покрытия кухонной утвари использовали кадмий, однако теперь известно, что этот металл опасен для здоровья и кадмиевые покрытия используются только в технике.
Для замедления коррозии на поверхность металла наносят лаки и краски, минеральные масла и смазку. Подземные конструкции покрывают толстым слоем битума или полиэтилена. Внутренние поверхности стальных труб и резервуаров защищают дешевыми покрытиями из цемента.
Чтобы лакокрасочное покрытие было более надежным, поверхность металла тщательно очищают от грязи и продуктов коррозии и подвергают специальной обработке. Для стальных изделий используют так называемые преобразователи ржавчины, содержащие ортофосфорную кислоту (Н 3 РО 4) и ее соли. Они растворяют остатки оксидов и формируют плотную и прочную пленку фосфатов, которая способна на некоторое время защитить поверхность изделия. Затем металл покрывают грунтовочным слоем, который должен хорошо ложиться на поверхность и обладать защитными свойствами (обычно используют свинцовый сурик или хромат цинка). Только после этого можно наносить лак или краску.
Одним из наиболее эффективных методов борьбы с коррозией является электрохимическая защита. Для защиты буровых платформ, сварных металлических оснований, подземных трубопроводов их подключают в качестве катода к внешнему источнику тока. В качестве анода используются вспомогательные инертные электроды.
Другой вариант такой защиты применяют для сравнительно небольших стальных конструкций или дополнительно покрытых изоляцией металлических объектов (например, трубопроводов). В этом случае используют протектор – анод из сравнительно активного металла (обычно это магний, цинк, алюминий и их сплавы), который постепенно разрушается, оберегая основной объект. С помощью одного магниевого анода защищают до 8 км трубопровода. Протекторная защита широко распространена; например, в США на производство протекторов ежегодно расходуется около 11,5 тыс. т алюминия.
Защита одного металла другим, более активным металлом, расположенным в ряду напряжений левее, эффективна и без наложения разности потенциалов. Более активный металл (например, цинк на поверхности железа) защищает от разрушения менее активный металл.
К электрохимическим методам борьбы с коррозией можно отнести и защиту от разрушения конструкций блуждающими токами. Одним из способов устранения такой коррозии является соединение металлическим проводником участка конструкции, с которого стекает блуждающий ток, с рельсом, по которому движется трамвай или электропоезд.
Елена Савинкина
физико-химическое или химическое взаимодействие между металлом (сплавом) и средой, приводящее к ухудшению функциональных свойств металла (сплава), среды или включающей их технической системы.Слово коррозия происходит от латинского «corrodo» «грызу» (позднелатинское «corrosio» означает «разъедание»).
Коррозия вызывается химической реакцией металла с веществами окружающей среды, протекающей на границе металла и среды. Чаще всего это окисление металла, например, кислородом воздуха или кислотами, содержащимися в растворах, с которыми контактирует металл. Особенно подвержены этому металлы, расположенные в ряду напряжений (ряду активности) левее водорода, в том числе железо.
В результате коррозии железо ржавеет. Этот процесс очень сложен и включает несколько стадий. Его можно описать суммарным уравнением:
Fe + 6 H 2 O (влага) + 3 O 2 (воздух) = 4 Fe (OH ) 3Гидроксид железа(
III ) очень неустойчив, быстро теряет воду и превращается в оксид железа(III ). Это соединение не защищает поверхность железа от дальнейшего окисления. В результате железный предмет может быть полностью разрушен.Многие металлы, в том числе и довольно активные (например, алюминий) при коррозии покрываются плотной, хорошо скрепленной с металлами оксидной пленкой, которая не позволяет окислителям проникнуть в более глубокие слои и потому предохраняет металл от коррозии. При удалении этой пленки металл начинает взаимодействовать с влагой и кислородом воздуха.
Алюминий в обычных условиях устойчив к воздействию воздуха и воды, даже кипящей, однако если на поверхность алюминия нанести ртуть, то образующаяся амальгама разрушает оксидную пленку выталкивает ее с поверхности, и металл быстро превращается в белые хлопья метагидроксида алюминия:
4Al + 2H 2 O + 3O 2 = 4AlO(OH) Амальгамированный алюминий взаимодействует с водой с выделением водорода: Al + 4 H 2 O = 2 AlO (OH ) + 3 H 2Коррозии подвергаются и некоторые довольно мало активные металлы. Во влажном воздухе поверхность меди покрывается зеленоватым налетом (патиной) в результате образования смеси основных солей.
Иногда при коррозии металлов происходит не окисление, а восстановление некоторых элементов, содержащихся в сплавах. Например, при высоких давлениях и температурах карбиды, содержащиеся в сталях, восстанавливаются водородом.
Разрушение металлов в присутствии водорода обнаружили в середине девятнадцатого века. Французский инженер Сент Клэр Девиль изучал причины неожиданных разрывов орудийных стволов. При их химическом анализе он нашел в металле водород. Девиль решил, что именно водородное насыщение явилось причиной внезапного падения прочности стали.
Много хлопот доставил водород конструкторам оборудования для одного из важнейших промышленных химических процессов синтеза аммиака. Первые аппараты для этого синтеза служили лишь десятки часов, а затем разлетались на мелкие части. Только добавление в сталь титана, ванадия или молибдена помогло решить эту проблему.
К коррозии металлов можно отнести также их растворение в жидких расплавленных металлах (натрий, свинец, висмут), которые используются, в частности, в качестве теплоносителей в ядерных реакторах.
По стехиометрии реакции, описывающие коррозию металлов, довольно просты, однако по механизму они относятся к сложным гетерогенным процессам. Механизм коррозии определяется, прежде всего, типом агрессивной среды.
При контакте металлического материала с химически активным газом на его поверхности появляется пленка продуктов реакции. Она препятствует дальнейшему контакту металла и газа. Если сквозь эту пленку происходит встречная диффузия реагирующих веществ, то реакция продолжается. Процесс облегчается при высоких температурах. В ходе коррозии пленка продукта непрерывно утолщается, а металл разрушается. Большие убытки от газовой коррозии терпит металлургия и другие отрасли промышленности, где используются высокие температуры.
Наиболее распространена коррозия в средах электролитов. В некоторых технологических процессах металлы контактируют с расплавами электролитов. Однако чаще всего коррозия протекает в растворах электролитов. Металл не обязательно должен быть полностью погружен в жидкость. Растворы электролитов могут находиться в виде тонкой пленки на поверхности металла. Они нередко пропитывают окружающую металл среду (почву, бетон и др.).
Во время строительства метромоста и станции «Ленинские горы» в Москве в бетон добавляли большое количество хлорида натрия, чтобы не допустить замерзания еще не схватившегося бетона. Станция была сооружена в кратчайшие сроки (всего за 15 месяцев) и открыта 12 января 1959. Однако присутствие хлорида натрия в бетоне вызвало разрушение стальной арматуры. Коррозии оказались подвергнуты 60% железобетонных конструкций, поэтому станция была закрыта на реконструкцию, продолжавшуюся почти 10 лет. Лишь 14 января 2002 состоялось повторное открытие метромоста и станции, получившей название «Воробьевы горы».
Использование солей (обычно хлорида натрия или кальция) для удаления снега и льда с дорог и тротуаров также приводит к ускоренному разрушению металлов. Сильно страдают транспортные средства и подземные коммуникации. Подсчитано, что только в США применение солей для борьбы со снегопадами и гололедом приводит к потерям на сумму около 2 млрд. долл. в год в связи с коррозией двигателей и 0,5 млрд. долл. на дополнительный ремонт дорог, подземных магистралей и мостов.
В средах электролитов коррозия обусловлена не только действием кислорода, воды или кислот на металлы, но и электрохимическими процессами. Уже в начале 19 в. электрохимическую коррозию изучали английские ученые Гемфри Дэви и Майкл Фарадей. Первая теория электрохимической коррозии была выдвинута в 1830 швейцарским ученым Де ла Ривом. Она объясняла возникновение коррозии в месте контакта двух разных металлов.
Электрохимическая коррозия приводит к быстрому разрушению более активных металлов, которые в различных механизмах и устройствах контактируют с менее активными металлами, расположенными в электрохимическом ряду напряжений правее. Использование медных или латунных деталей в железных или алюминиевых конструкциях, которые работают в морской воде, существенно усиливает коррозию. Известны случаи разрушения и затопления кораблей, железная обшивка которых была скреплена медными заклепками.
По отдельности алюминий и титан устойчивы к действию морской воды, но если они контактируют в одном изделии, например в боксе для подводной фототехники, алюминий очень быстро разрушается, и бокс протекает.
Электрохимические процессы могут протекать и в однородном металле. Они активизируются, если есть различия в составе зерна металла в объеме и на границе, неоднородное механическое напряжение, микропримеси и т.д. В разработке общей теории электрохимической коррозии металлических материалов участвовали многие наши соотечественники, в том числе Владимир Александрович Кистяковский (18651952) и Александр Наумович Фрумкин (18951976).
Одной из причин возникновения электрохимической коррозии являются блуждающие токи, которые появляются вследствие утечки части тока из электрических цепей в почву или водные растворы, где они попадают на металлические конструкции. В местах выхода тока из этих конструкций вновь в почву или воду начинается растворение металла. Такие зоны разрушения металлов под действием блуждающих токов особенно часто наблюдаются в районах наземного электрического транспорта (трамвайные линии, железнодорожный транспорт на электрической тяге). Эти токи могут достигать несколько ампер, что приводит к большим коррозионным разрушениям. Например, прохождение тока силой в 1 А в течение одного года вызовет растворение 9,1 кг железа, 10,7 кг цинка, 33,4 кг свинца.
Коррозия может возникать и под влиянием радиационного излучения, а также продуктов жизнедеятельности бактерий и других организмов. С развитием бактерий на поверхности металлических конструкций связано явление биокоррозии. Обрастание подводной части судов мелкими морскими организмами также оказывает влияние на коррозионные процессы.
При одновременном воздействии на металл внешней среды и механических напряжений все коррозионные процессы активизируются, поскольку при этом понижается термическая устойчивость металла, нарушаются оксидные пленки на поверхности металла, усиливаются электрохимические процессы в местах появления трещин и неоднородностей.
Коррозия приводит к огромным безвозвратным потерям металлов, ежегодно полностью разрушается около 10% производимого железа. По данным Института физической химии РАН, каждая шестая домна в России работает впустую весь выплавляемый металл превращается в ржавчину. Разрушение металлических конструкций, сельскохозяйственных и транспортных машин, промышленной аппаратуры становится причиной простоев, аварий, ухудшения качества продукции. Учет возможной коррозии приводит к повышенным затратам металла при изготовлении аппаратов высокого давления, паровых котлов, металлических контейнеров для токсичных и радиоактивных веществ и т.д. Это увеличивает общие убытки от коррозии. Немалые средства приходится тратить на противокоррозионную защиту. Соотношение прямых убытков, косвенных убытков и расходов на защиту от коррозии оценивают как (34):1:1. В промышленно развитых странах ущерб от коррозии достигает 4% национального дохода. В нашей стране он исчисляется миллиардами рублей в год.
Проблемы коррозии постоянно обостряются из-за непрерывного роста производства металлов и ужесточения условий их эксплуатации. Среда, в которой используются металлические конструкции, становится все более агрессивной, в том числе и за счет ее загрязнения. Металлические изделия, используемые в технике, работают в условиях все более высоких температур и давлений, мощных потоков газов и жидкостей. Поэтому вопросы защиты металлических материалов от коррозии становятся все более актуальными. Полностью предотвратить коррозию металлов невозможно, поэтому единственным путем борьбы с ней является поиск способов ее замедления.
Проблема защиты металлов от коррозии возникла почти в самом начале их использования. Люди пытались защитить металлы от атмосферного воздействия с помощью жира, масел, а позднее и покрытием другими металлами и, прежде всего, легкоплавким оловом (лужением). В трудах древнегреческого историка Геродота (5 в. до н. э.) и древнеримского ученого Плиния Старшего (1 в. до н. э.) уже есть упоминания о применении олова для предохранения железа от ржавления. В настоящее время борьбу с коррозией ведут сразу в нескольких направлениях пытаются изменить среду, в которой работает металлическое изделие, повлиять на коррозионную устойчивость самого материала, предотвратить контакт между металлом и агрессивными веществами внешней среды.
Полностью предотвратить коррозию можно только в инертной среде, например в атмосфере аргона, однако реально создать такую среду при эксплуатации конструкций и механизмов в подавляющем большинстве случаев невозможно. На практике для снижения коррозионной активности среды из нее стараются удалить наиболее реакционноспособные компоненты, например, снижают кислотность водных растворов и почв, с которыми могут контактировать металлы. Одним из методов борьбы с коррозией железа и его сплавов, меди, латуни, цинка, свинца является удаление из водных растворов кислорода и диоксида углерода. В энергетике и некоторых отраслях техники воду освобождают также от хлоридов, которые стимулируют локальную коррозию. Для снижения кислотности почвы проводят известкование.
Агрессивность атмосферы сильно зависит от влажности. Для любого металла есть некоторая критическая относительная влажность, ниже которой он не подвергается атмосферной коррозии. Для железа, меди, никеля, цинка она составляет 5070%. Иногда для сохранности изделий, имеющих историческую ценность, их температуру искусственно поддерживают выше точки росы. В закрытых пространствах (например, в упаковочных коробках) влажность понижают с помощью силикагеля или других адсорбентов. Агрессивность промышленной атмосферы определяется, в основном продуктами сгорания топлива (см . ЗАГРЯЗНЕНИЕ ОКРУЖАЮЩЕЙ СРЕДЫ ). Уменьшению потерь от коррозии способствует предотвращение кислотных дождей и устранение вредных газовых выбросов.
Разрушение металлов в водных средах можно замедлить при помощи ингибиторов коррозии, которые в небольших количествах (обычно менее 1%) вводят в водные растворы. Они способствуют пассивированию поверхности металла, то есть образованию тонкой и плотной пленки оксидов или других малорастворимых соединений, которая препятствует разрушению основного вещества. Для этой цели применяют некоторые соли натрия (карбонат, силикат, борат) и другие соединения. Если бритвенные лезвия погрузить в раствор хромата калия, они хранятся намного дольше. Часто используют органические ингибиторы, которые более эффективны, чем неорганические.
Один из способов защиты от коррозии основывается на разработке новых материалов, обладающих более высокой коррозионной стойкостью. Постоянно ведутся поиски заменителей коррозирующих металлов. Пластмассы, керамика, стекло, резина, асбест и бетон более устойчивы к воздействию окружающей среды, однако по многим другим свойствам они уступают металлам, которые по-прежнему служат основными конструкционными материалами.
Благородные металлы практически не поддаются коррозии, но для широкого применения они слишком дороги, поэтому их используют лишь в наиболее ответственных деталях, например для изготовления некорродирующих электрических контактов. Высокой коррозионной стойкостью обладают никель, алюминий, медь, титан и сплавы на их основе. Их производство растет довольно быстро, однако и сейчас наиболее доступным и широко используемым металлом остается быстро ржавеющее железо. Для придания коррозионной стойкости сплавам на основе железа часто используют легирование. Так получают нержавеющую сталь, которая, помимо железа, содержит хром и никель. Самая распространенная в наше время нержавеющая сталь марки 188 (18% хрома и 8% никеля) появилась в 1923. Она вполне устойчива к воздействию влаги и кислорода. Первые тонны нержавеющей стали в нашей стране были выплавлены в 1924 в Златоусте. Сейчас разработано много марок таких сталей, которые, помимо хрома и никеля, содержат марганец, молибден, вольфрам и другие химические элементы. Часто применяют поверхностное легирование недорогих железных сплавов цинком, алюминием, хромом.
Для противостояния атмосферной коррозии на стальные изделия наносятся тонкие покрытия из других металлов, более устойчивых к воздействию влаги и кислорода воздуха. Часто используются покрытия из хрома и никеля. Поскольку хромовые покрытия нередко содержат трещины, их обычно наносят поверх менее декоративных никелевых покрытий. На защиту жестяных консервных банок от коррозии в органических кислотах, содержащихся в пищевых продуктах, расходуется значительное количество олова. Долгое время для покрытия кухонной утвари использовали кадмий, однако теперь известно, что этот металл опасен для здоровья и кадмиевые покрытия используются только в технике.
Для замедления коррозии на поверхность металла наносят лаки и краски, минеральные масла и смазку. Подземные конструкции покрывают толстым слоем битума или полиэтилена. Внутренние поверхности стальных труб и резервуаров защищают дешевыми покрытиями из цемента.
Чтобы лакокрасочное покрытие было более надежным, поверхность металла тщательно очищают от грязи и продуктов коррозии и подвергают специальной обработке. Для стальных изделий используют так называемые преобразователи ржавчины, содержащие ортофосфорную кислоту (Н 3 РО 4) и ее соли. Они растворяют остатки оксидов и формируют плотную и прочную пленку фосфатов, которая способна на некоторое время защитить поверхность изделия. Затем металл покрывают грунтовочным слоем, который должен хорошо ложиться на поверхность и обладать защитными свойствами (обычно используют свинцовый сурик или хромат цинка). Только после этого можно наносить лак или краску.
Одним из наиболее эффективных методов борьбы с коррозией является электрохимическая защита. Для защиты буровых платформ, сварных металлических оснований, подземных трубопроводов их подключают в качестве катода к внешнему источнику тока. В качестве анода используются вспомогательные инертные электроды.
Другой вариант такой защиты применяют для сравнительно небольших стальных конструкций или дополнительно покрытых изоляцией металлических объектов (например, трубопроводов). В этом случае используют протектор анод из сравнительно активного металла (обычно это магний, цинк, алюминий и их сплавы), который постепенно разрушается, оберегая основной объект. С помощью одного магниевого анода защищают до 8 км трубопровода. Протекторная защита широко распространена; например, в США на производство протекторов ежегодно расходуется около 11,5 тыс. т алюминия.
Защита одного металла другим, более активным металлом, расположенным в ряду напряжений левее, эффективна и без наложения разности потенциалов. Более активный металл (например, цинк на поверхности железа) защищает от разрушения менее активный металл.
К электрохимическим методам борьбы с коррозией можно отнести и защиту от разрушения конструкций блуждающими токами. Одним из способов устранения такой коррозии является соединение металлическим проводником участка конструкции, с которого стекает блуждающий ток, с рельсом, по которому движется трамвай или электропоезд.
Елена Савинкина
ЛИТЕРАТУРА Фримантл М. Химия в действии . В 2-х ч. М., Мир, 1991Степин Б.Д., Аликберова Л.Ю. Книга по химии для домашнего чтения . М., Химия, 1994
Министерство образования Российской Федерации
Тихоокеанский Государственный Экономический Университет
РЕФЕРАТ
Дисциплина:Химия
Тема: Коррозия металлов
Выполнил:
Студентка 69группы
Кривицкая Евгения
Находка
Коррозия неметаллических материалов
По мере ужесточения условий эксплуатации (повышение температуры, механических напряжений, агрессивности среды и др.) и неметаллические материалы подвержены действию среды. В связи с чем термин «коррозия» стал применяться и по отношению к этим материалам, например «коррозия бетонов и железобетонов», «коррозия пластмасс и резин». При этом имеется в виду их разрушение и потеря эксплуатационных свойств в результате химического или физико-химического взаимодействия с окружающей средой. Но следует учитывать, что механизмы и кинетика процессов для неметаллов и металлов будут разными.
Коррозия металлов
Образование гальванических пар с пользой применяют для создания батарей и аккумуляторов. С другой стороны, образование такой пары приводит к неблагоприятному процессу, жертвой которого становится целый ряд металлов, - коррозии. Под коррозией понимают происходящее на поверхности электрохимическое или химическое разрушение металлического материала. Наиболее часто при коррозии металл окисляется с образованием ионов металла, которые при дальнейших превращениях дают различные продукты коррозии. Коррозия может быть вызвана как химическим, так и электрохимическим процессом. Соответственно, различают химическую и электрохимическую коррозию металлов.
Химическая коррозия
Химическая коррозия - взаимодействие поверхности металла с (коррозионно-активной ) средой, не сопровождающееся возникновением электрохимических процессов на границе фаз. В этом случае взаимодействия окисление металла и восстановление окислительного компонента коррозионной среды протекают в одном акте. Например, образование окалины при взаимодействии материалов на основе железа при высокой температуре с кислородом:
4Fe + 3O 2 → 2Fe 2 O 3
При электрохимической коррозии ионизация атомов металла и восстановление окислительного компонента коррозионной среды протекают не в одном акте и их скорости зависят от электродного потенциала металла (например, ржавление стали в морской воде).
Электрохимическая коррозия
Разрушение металла под воздействием возникающих в коррозионной среде гальванических элементов называют электрохимической коррозией. Не следует путать с электрохимической коррозией коррозию однородного материала, например, ржавление железа или т.п. При электрохимической коррозии (наиболее частая форма коррозии) всегда требуется наличие электролита (Конденсат, дождевая вода и т. д.), с которым соприкасаются электроды - либо различные элементы структуры материала, либо два различных соприкасающихся материала с различающимися окислительно-восстановительными потенциалами. Если в воде растворены ионы солей, кислот, или т.п., электропроводность ее повышается, и скорость процесса увеличивается.
Коррозионный элемент
При соприкосновении двух металлов с различными окислительно-восстановительными потенциалами и погружении их в раствор электролита, например, дождевой воды с растворенным углекислым газом CO 2 , образуется гальванический элемент, так называемый коррозионный элемент. Он представляет собой не что иное, как замкнутую гальваническую ячейку. В ней происходит медленное растворение металлического материала с более низким окислительно-восстановительным потенциалом; второй электрод в паре, как правило, не корродирует. Этот вид коррозии особо присущ металлам с высокими отрицательными потенциалами. Так, совсем небольшого количества примеси на поверхности металла с большим редокспотенциалом уже достаточно для возникновения коррозионного элемента. Особо подвержены риску места соприкосновения металлов с различными потенциалами, например, сварочные швы или заклёпки.
Если растворяющийся электрод коррозионно-стоек, процесс коррозии замедляется. На этом основана, например, защита железных изделий от коррозии путём лужения или оцинковки - олово или цинк имеют более отрицательный потенциал, чем железо, поэтому в такой паре железо восстанавливается, а олово или цинк должны корродировать. Однако в связи с образованием на поверхности олова или цинка окисной плёнки процесс коррозии сильно замедляется.
Водородная и кислородная коррозия
Если происходит восстановление ионов H 3 O + или молекул воды H 2 O, говорят о водородной коррозии или коррозии с водородной деполяризацией. Восстановление ионов происходит по следующей схеме:
2H 3 O + + 2e − → 2H 2 O + H 2
2H 2 O + 2e − → 2OH − + H 2
Если водород не выделяется, что часто происходит в нейтральной или сильно щелочной среде, происходит восстановление кислорода и здесь говорят о кислородной коррозии или коррозии с кислородной деполяризацией:
O 2 + 2H 2 O + 4e − → 4OH −
Коррозионный элемент может образовываться не только при соприкосновении двух различных металлов. Коррозионный элемент образуется и в случае одного металла, если, например, структура поверхности неоднородна.
Борьба с коррозией
Коррозия приводит ежегодно к миллиардным убыткам, и разрешение этой проблемы является важной задачей. Основной ущерб, причиняемый коррозией, заключается не в потере металла как такового, а в огромной стоимости изделий, разрушаемых коррозией. Вот почему ежегодные потери от неё в промышленно развитых странах столь велики. Истинные убытки от неё нельзя определить, оценив только прямые потери, к которым относятся стоимость разрушившейся конструкции, стоимость замены оборудования, затраты на мероприятия по защите от коррозии. Ещё больший ущерб составляют косвенные потери. Это простои оборудования при замене прокорродировавших деталей и узлов, утечка продуктов, нарушение технологических процессов.
Идеальная защита от коррозии на 80 % обеспечивается правильной подготовкой поверхности, и только на 20 % качеством используемых лакокрасочных материалов и способом их нанесения. . Наиболее производительным и эффективным методом подготовки поверхности перед дальнейшей защитой субстрата является абразивоструйная очистка .
Обычно выделяют три направления методов защиты от коррозии:
1. Конструкционный
2. Активный
3. Пассивный
Для предотвращения коррозии в качестве конструкционных материалов применяют нержавеющие стали , кортеновские стали , цветные металлы .
В качестве защиты от коррозии может применяться нанесение какого-либо покрытия , которое препятствует образованию коррозионного элемента (пассивный метод).
Кислородная коррозия оцинкованного железа
Кислородная коррозия железа, покрытого оловом
Красочное покрытие, полимерное покрытие и эмалирование должны, прежде всего, предотвратить доступ кислорода и влаги. Часто также применяется покрытие, например, стали другими металлами, такими как цинк, олово, хром, никель. Цинковое покрытие защищает сталь даже когда покрытие частично разрушено. Цинк имеет более отрицательный потенциал и корродирует первым. Ионы Zn 2+ токсичны. При изготовлении консервных банок применяют жесть, покрытую слоем олова. В отличие от оцинкованной жести, при разрушении слоя олова корродировать, притом усиленно, начинает железо, так как олово имеет более положительный потенциал. Другая возможность защитить металл от коррозии - применение защитного электрода с большим отрицательным потенциалом, например, из цинка или магния. Для этого специально создаётся коррозионный элемент. Защищаемый металл выступает в роли катода, и этот вид защиты называют катодной защитой. Растворяемый электрод, называют, соответственно, анодом протекторной защиты Этот метод применяют для защиты от коррозии морских судов, мостов, котельных установок, расположенных под землей труб. Для защиты корпуса судна на наружную сторону корпуса крепят цинковые пластинки.
Если сравнить потенциалы цинка и магния с железом, они имеют более отрицательные потенциалы. Но тем не менее корродируют они медленнее вследствие образования на поверхности защитной оксидной плёнки, которая защищает металл от дальнейшей коррозии. Образование такой плёнки называют пассивацией металла. У алюминия её усиливают анодным окислением (анодирование). При добавлении небольшого количества хрома в сталь на поверхности металла образуется оксидная плёнка. Содержание хрома в нержавеющей стали - более 12 процентов.
Система холодного цинкования
Система холодного цинкования предназначена для усиления антикоррозионных свойств комплексного многослойного покрытия. Система обеспечивает полную катодную (или гальваническую) защиту железных поверхностей от коррозии в различных агрессивных средах
Система холодной оцинковки бывает одно-, двух- или трехупаковочной и включает:
· связующее - известны составы на хлоркаучуковой, этилсиликатной, полистирольной, эпоксидной, уретановой, алкидной (модифицированной) основе;
· антикоррозионный наполнитель - цинковый порошок («цинковая пыль»), с содержанием более 95 % металлического цинка, имеющего размер частиц менее 10 мкм и минимальную степень окисления.;
· отвердитель (в двух- и трех- упаковочных системах)
Одноупаковочные системы холодного цинкования поставляютмся готовыми к применению и требуют лишь тщательного перемешивания состава перед нанесением. Двух- и трехупаковочные системы могут поставляться в нескольких упаковках и требуют дополнительных операций по приготовлению состава перед нанесением (смешивание связующего, наполнителя, отвердителя).


Коррозия металла или сплава происходит, как правило, на границе раздела фаз, т. е. на границе соприкосновения твердого вещества с газом или жидкостью.
Коррозионные процессы подразделяются на следующие виды: по механизму взаимодействия металла со средой; по виду коррозионной среды; по виду коррозионных разрушений поверхности; по объему разрушенного металла; по характеру дополнительных воздействий, которым подвергается металл одновременно с действием коррозионной среды.
По механизму взаимодействия металла со средой различают химическую и электрохимическую коррозию.
Коррозию, протекающую под влиянием жизнедеятельности микроорганизмов, относят к биологической коррозии, а протекающую под действием радиоактивного излучения - к радиационной коррозии.
По виду коррозионной среды, участвующей в коррозионном разрушении металла или сплава, различают коррозию в жидкостях-неэлектролитах, коррозию в растворах и расплавах электролитов, газовую, атмосферную, подземную (почвенную) коррозию, коррозию блуждающим током и др.
По характеру изменения поверхности металла или сплава или по степени изменения их физико-механических свойств, в процессе коррозии независимо от свойств, среды коррозионные разрушения бывают нескольких видов.
1. Если коррозия охватывает всю поверхность металла, то такой вид разрушения называется - сплошной коррозией . К сплошной коррозии относится разрушение металлов и сплавов под действием кислот, щелочей, атмосферы. Сплошная коррозия может быть равномерной, т. е. разрушение металла происходит с одинаковой скоростью по всей поверхности, и неравномерной, когда скорость коррозии на отдельных участках поверхности неодинакова. Примером равномерной коррозии может служить коррозия при взаимодействии меди с азотной, железа - с соляной, цинка - с серной кислотами, алюминия - с растворами щелочей. В этих случаях продукты коррозии не остаются на поверхности металла. Аналогично коррозируют железные трубы на открытом воздухе. Это легко увидеть, если удалить слой ржавчины; под ним обнаруживается шероховатая поверхность металла, равномерно распределенная по всей трубе.
2. Сплавы некоторых металлов подвержены - избирательной коррозии , когда один из элементов или одна из структур сплава разрушается, а остальные практически остаются без изменений. При соприкосновении латуни с серной кислотой происходит компонентно-избирательная коррозия - коррозия цинка, а сплав обогащается медью. Такое разрушение легко заметить, так как происходит покраснение поверхности изделия за счет увеличения концентрации меди в сплаве. При структурно-избирательной коррозии происходит преимущественно разрушение какой-либо одной структуры сплава, так, например, при соприкосновении стали с кислотами феррит разрушается, а карбид железа остается без изменений. Этому виду коррозии особенно подвержены чугуны.
3. При местной коррозии на поверхности металла обнаруживаются поражения в виде отдельных пятен, язв, точек. В зависимости от характера поражений местная коррозия бывает в виде пятен, т. е. поражений, не сильно углубленных в толщу металла; язв - поражений, сильно углубленных в толщу металла; точек, иногда еле заметных глазу, но глубоко проникающих в металл. Коррозия в виде язв и точек очень опасна для таких конструкций, где важно поддерживать условия герметичности и непроницаемости (емкости, аппараты, трубопроводы, применяемые в химической промышленности).
4. Подповерхностная коррозия начинается с поверхности металла в тех случаях, когда защитное покрытие (пленки, оксиды и т. п.) разрушено на отдельных участках. В этом случае разрушение идет преимущественно под покрытием, и продукты коррозии сосредотачиваются внутри металла. Подповерхностная коррозия часто вызывает вспучивание и расслоение металла. Определить ее возможно только под микроскопом.
5. Щелевая коррозия - разрушение металла под прокладками, в зазорах, резьбовых креплениях, в клепаных соединениях и т. п. Она чаще развивается на участке конструкции, находящейся в зазоре (щели).
6. Межкристаллитная коррозия - разрушение металла по границам кристаллитов (зерен) с потерей его механической прочности, внешний вид металла при этом не меняется, но он легко разрушается на отдельные кристаллики под механическим воздействием. Объясняется это образованием между зернами металла или сплава рыхлых, малопрочных продуктов коррозии. Этому виду коррозии подвержены хромистые и хромоникелевые стали, никелевые и алюминиевые сплавы. Чтобы избежать межкристаллитной коррозии, в последние годы широко используют нержавеющие стали с пониженным содержанием углерода или в их состав вводят карбидообразователи - титан, тантал, ниобий (в 5-8 - кратном количестве от содержания углерода).
При одновременном воздействии на металл или сплав сильно агрессивных сред и механических растягивающих напряжений возможно коррозионное растрескивание, или транскристаллитная коррозия. В этом случае разрушение происходит не только по границам кристаллитов, но разделяется на части сам кристаллит металла. Это очень опасный вид коррозии, особенно для конструкций, несущих механические нагрузки (мосты, оси, тросы, рессоры, автоклавы, паровые котлы, двигатели внутреннего сгорания, водяные и паровые турбины и др.).
Коррозионное растрескивание зависит от конструкции аппаратуры, характера агрессивной среды, строения и структуры металла или сплава, температуры и т. д. Например, коррозионное растрескивание углеродистых сталей очень часто происходит в щелочных средах при высоких температурах; нержавеющих сталей - в растворах хлоридов, медного купороса, ортофосфорной кислоты; алюминиевых и магниевых сплавов - под действием морской воды; титана и его сплавов - под действием концентрированной азотной кислоты и растворов йода в метаноле.
Следует отметить, что в зависимости от природы металла или сплава и свойств агрессивной среды существует критическое напряжение, выше которого коррозионное растрескивание наблюдается часто.
По характеру дополнительных воздействий, которым подвергается металл, одновременно с воздействием агрессивной среды можно выделить коррозию под напряжением, коррозию при трении и кавитационную.
7. Коррозия под напряжением - это коррозия при одновременном воздействии коррозионной среды и постоянных или временных напряжений. Одновременное воздействие циклических растягивающих напряжений и коррозионной среды вызывает коррозионную усталость, т. е. Происходит преждевременное разрушение металла. Этот процесс можно представить следующим образом: сначала на поверхности изделия возникает местная коррозия в виде язв, которые начинают действовать в качестве концентратора напряжений, максимальное значение напряжения будет на дне язв, которое имеет более отрицательный потенциал, чем стенки, в результате чего разрушение металла будет идти вглубь, а язва будет переходить в трещину. Этому виду коррозии подвержены валы гребных винтов. Рессоры автомобилей, канаты, охлаждаемые валки прокатных станов и др.
8. Коррозия при трении - разрушение металла, вызываемое одновременным воздействием коррозионной среды и трения. При колебательном перемещении двух поверхностей относительно друг друга в условиях воздействия коррозионной среды происходит коррозия истиранием, или фреттинг-коррозия. Устранить коррозию при трении или вибрации возможно правильным выбором конструкционного материала, снижением коэффициента трения, применением покрытий и т.д.
9. Газовая коррозия - это химическая коррозия металлов в газовой среде при минимальном содержании влаги (как правило не более 0,1%) или при высоких температурах. В химической и нефтехимической промышленности такой вид коррозии встречается часто. Например, при получении серной кислоты на стадии окисления диоксида серы, при синтезе аммиака, получении азотной кислоты и хлористого водорода, в процессах синтеза органических спиртов, крекинга нефти и т.д.
10. Атмосферная коррозия - это коррозия металлов в атмосфере воздуха или любого влажного газа.
11. Подземная коррозия - это коррозия металлов в почвах и грунтах.
12. Контактная коррозия - это вид коррозии, вызванный контактом металлов, имеющих разные стационарные потенциалы в данном электролите.