Основные положения молекулярно-кинетической теории. Молекулярно-кинетическая теория
Данный видеоурок посвящен теме «Основные положения МКТ. Строение вещества. Молекула». Здесь вы узнаете, что изучает молекулярно-кинетическая теория (МКТ) в физике. Познакомитесь с тремя основными положениями, на которых базируется МКТ. Узнаете, чем определяются физические свойства вещества и что представляют собой атом и молекула.
Для начала давайте вспомним все предыдущие разделы физики, которые мы изучали, и поймём, что всё это время мы рассматривали процессы, происходящие с макроскопическими телами (или объектами макромира). Теперь же мы будем изучать их строение и процессы, протекающие внутри них.
Определение. Макроскопическое тело - тело, состоящее из большого числа частиц. Например: машина, человек, планета, бильярдный шар…
Микроскопическое тело - тело, состоящее из одной или нескольких частиц. Например: атом, молекула, электрон… (рис. 1)

Рис. 1. Примеры микро- и макрообъектов соответственно
Определив таким образом предмет изучения курса МКТ, следует теперь поговорить об основных целях, которые ставит перед собой курс МКТ, а именно:
- Изучение процессов, происходящих внутри макроскопического тела (движение и взаимодействие частиц)
- Свойства тел (плотность, масса, давление (для газов)…)
- Изучение тепловых явлений (нагревание-охлаждение, изменения агрегатных состояний тела)
Изучение этих вопросов, которое будет проходить на протяжении всей темы, начнётся сейчас с того, что мы сформулируем так называемые основные положения МКТ, то есть некоторые утверждения, истинность которых уже давно не подвергается сомнениям, и, отталкиваясь от которых, будет строиться весь дальнейший курс.
Разберём их по очереди:
Все вещества состоят из большого количества частиц - молекул и атомов.
Определение. Атом - мельчайшая частица химического элемента. Размеры атомов (их диаметр) имеет порядок см. Стоит отметить, что различных типов атомов, в отличие от молекул, относительно немного. Все их разновидности, которые на сегодняшний день известны человеку, собраны в так называемой таблице Менделеева (см. рис. 2)

Рис. 2. Периодическая таблица химических элементов (по сути разновидностей атомов) Д. И. Менделеева
Молекула - структурная единица вещества, состоящая из атомов. В отличие от атомов, они больше и тяжелее последних, а главное, они обладают огромным разнообразием.
Вещество, молекулы которого состоят из одного атома, называются атомарными , из большего количества - молекулярными . Например: кислород, вода, поваренная соль () - молекулярные; гелий серебро (He, Ag) - атомарные.
Причём следует понимать, что свойства макроскопических тел будут зависеть не только от количественной характеристики их микроскопического состава, но и от качественной.

Если в строении атомов вещество имеет какую-то определённую геометрию (кристаллическую решётку ), или же, наоборот, не имеет, то этим телам будут присущи различные свойства. Например, аморфные тела не имеют строгой температуры плавления. Самый известный пример - это аморфный графит и кристаллический алмаз. Оба вещества состоят из атомов углерода.


Рис. 3. Графит и алмаз соответственно
Таким образом «из скольких, в каком взаимном расположении и каких атомов и молекул состоит вещество?» - первый вопрос, ответ на который приблизит нас к пониманию свойств тел.
Все упомянутые выше частицы находятся в непрерывном тепловом хаотическом движении.
Так же, как и в рассматриваемых выше примерах, важно понимание не только количественных аспектов этого движения, но и качественных для различных веществ.
Молекулы и атомы твёрдых тел совершают лишь небольшие колебания относительно своего постоянного положения; жидких - также совершают колебания, но из-за больших размеров межмолекулярного пространства иногда меняются местами друг с другом; частички газа, в свою очередь, практически не сталкиваясь, свободно перемещаются в пространстве.
Частицы взаимодействуют друг с другом.
Взаимодействие это носит электромагнитный характер (взаимодействия ядер и электронов атома) и действует в обе стороны (как притягивание, так и отталкивание).

Здесь: d - расстояние между частицами; a - размеры частиц (диаметр).
Впервые понятие «атом» было введено древнегреческим философом и естествоведом Демокритом (рис. 4). В более поздний период активно задался вопросом о структуре микромира русский учёный Ломоносов (рис. 5).

Рис. 4. Демокрит

Рис. 5. Ломоносов
На следующем занятии мы введём методы качественного обоснования основным положениям МКТ.
Список литературы
- Мякишев Г.Я., Синяков А.З. Молекулярная физика. Термодинамика. - М.: Дрофа, 2010.
- Генденштейн Л.Э., Дик Ю.И. Физика 10 класс. - М.: Илекса, 2005.
- Касьянов В.А. Физика 10 класс. - М.: Дрофа, 2010.
- Elementy.ru ().
- Samlib.ru ().
- Youtube ().
Домашнее задание
- *Благодаря какой силе возможно сделать эксперимент по измерению размеров молекулы масла, показанный в видеоуроке?
- Почему молекулярно-кинетическая теория не рассматривает органические соединения?
- Почему даже очень маленькая песчинка песка является объектом макромира?
- Силы преимущественно какой природы действуют на частицы со стороны других частиц?
- Как определить, является ли некая химическая структура химическим элементом?
Молекулярно-кинетическая теория (сокращённо МКТ) - теория, возникшая в XIX веке и рассматривающая строение вещества, в основном газов, с точки зрения трёх основных приближенно верных положений:
все тела состоят из частиц: атомов , молекул и ионов ;
частицы находятся в непрерывном хаотическом движении (тепловом);
частицы взаимодействуют друг с другом путём абсолютно упругих столкновений .
МКТ стала одной из самых успешных физических теорий и была подтверждена целым рядом опытных фактов. Основными доказательствами положений МКТ стали:
Диффузия
Броуновское движение
Изменение агрегатных состояний вещества
На основе МКТ развит целый ряд разделов современной физики, в частности, физическая кинетика и статистическая механика . В этих разделах физики изучаются не только молекулярные (атомные или ионные) системы, находящиеся не только в «тепловом» движении, и взаимодействующие не только через абсолютно упругие столкновения. Термин же молекулярно-кинетическая теория в современной теоретической физике уже практически не используется, хотя он встречается в учебниках по курсу общей физики.
Идеальный газ - математическая модель газа , в которой предполагается, что: 1) потенциальной энергией взаимодействия молекул можно пренебречь по сравнению с их кинетической энергией ; 2) суммарный объем молекул газа пренебрежимо мал. Между молекулами не действуют силы притяжения или отталкивания, соударения частиц между собой и со стенками сосуда абсолютно упруги , а время взаимодействия между молекулами пренебрежимо мало по сравнению со средним временем между столкновениями. В расширенной модели идеального газа частицы, из которого он состоит, имеют также форму в виде упругих сфер или эллипсоидов , что позволяет учитывать энергию не только поступательного, но и вращательно-колебательного движения, а также не только центральные, но и нецентральные столкновения частиц и др.
Различают классический идеальный газ (его свойства выводятся из законов классической механики и описываются статистикой Больцмана) и квантовый идеальный газ (свойства определяются законами квантовой механики, описываются статистиками Ферми - Дирака или Бозе - Эйнштейна )
Классический идеальный газ
Объём идеального газа линейно зависит от температуры при постоянном давлении
Свойства идеального газа на основе молекулярно-кинетических представлений определяются исходя из физической модели идеального газа, в которой приняты следующие допущения:
В этом случае частицы газа движутся независимо друг от друга, давление газа на стенку равно полному импульсу, переданному при столкновении частиц со стенкой в единицу времени, внутренняя энергия - сумме энергий частиц газа.
По эквивалентной формулировке идеальный газ - такой газ, который одновременно подчиняется закону Бойля - Мариотта и Гей-Люссака , то есть:
где - давление,- абсолютная температура. Свойства идеального газа описываютсяуравнением Менделеева - Клапейрона
![]() ,
,
где -, - масса,-молярная масса .
где -концентрация частиц , -постоянная Больцмана .
Для любого идеального газа справедливо соотношение Майера :
![]()
где -универсальная газовая постоянная , - молярнаятеплоемкость при постоянном давлении, - молярная теплоемкость при постоянном объёме.
Статистический расчет распределения скоростей молекул был выполнен Максвеллом.
Рассмотрим результат, полученный Максвеллом в виде графика.
Молекулы газа при своем движении постоянно сталкиваются. Скорость каждой молекулы при столкновении изменяется. Она может возрастать и убывать. Однако среднеквадратичная скорость остается неизменной. Это объясняется тем, что в газе, находящемся при определенной температуре, устанавливается некоторое стационарное, не меняющееся со временем распределение молекул по скоростям, которое подчиняется определенному статистическому закону. Скорость отдельной молекулы с течением времени может меняться, однако доля молекул со скоростями в некотором интервале скоростей остается неизменной.
Нельзя ставить вопрос: сколько молекул обладает определенной скоростью. Дело в том, что, хоть число молекул очень велико в любом даже малом объеме, но количество значений скорости сколь угодно велико (как чисел в последовательном ряде), и может случиться, что ни одна молекула не обладает заданной скоростью.
|
|
Основываясь на опыте Штерна, можно ожидать, что наибольшее число молекул будут иметь какую-то среднюю скорость, а доля быстрых и медленных молекул не очень велика. Необходимые измерения показали, что доля молекул , отнесенная к интервалу скорости Δv , т.е. , имеет вид, показанный на рис. 3.3. Максвелл в 1859 г. теоретически на основании теории вероятности определил эту функцию. С тех пор она называется функцией распределения молекул по скоростям или законом Максвелла.

Выведем
функцию распределения молекул идеального
газа по скоростям

 -
интервал скоростей вблизи скорости
-
интервал скоростей вблизи скорости
 .
.
 -
число молекул, скорости которых лежат
в интервале
-
число молекул, скорости которых лежат
в интервале
 .
.
 -
число молекул в рассматриваемом объеме.
-
число молекул в рассматриваемом объеме.
 -
угол молекул, скорости которых принадлежат
интервалу
-
угол молекул, скорости которых принадлежат
интервалу
 .
.
 -
доля молекул в единичном интервале
скоростей вблизи скорости
-
доля молекул в единичном интервале
скоростей вблизи скорости
 .
.
 -
формула Максвелла.
-
формула Максвелла.
Используя статистические методы Максвелла получим следующую формулу:
 .
.
 -
масса одной молекулы,
-
масса одной молекулы,
 - постоянная Больцмана.
- постоянная Больцмана.
Наивероятнейшая
скорость определяется из условия
 .
.
Решая
получаем
 ;
; .
.
Обозначим
ч/з
 .
.
Тогда
 .
.
Рассчитаем долю молекул в заданном интервале скоростей вблизи заданной скорости в заданном направлении.
 .
.
 .
.
 -
доля молекул, которые имеют скорости в
интервале
-
доля молекул, которые имеют скорости в
интервале
 ,
, ,
, .
.
Развивая идеи Максвелла Больцман рассчитал распределение молекул по скоростям в силовом поле. В отличие от распределения Максвелла в распределении Больцмана вместо кинетической энергии молекул фигурирует сумма кинетической и потенциальной энергии.
В
распределении Максвелла:
 .
.
В
распределении Больцмана:
 .
.
В
гравитационном поле

 .
.
Для концентрации молекул идеального газа имеет место формула:


 и
и соответственно.
соответственно.
 -
распределение Больцмана.
-
распределение Больцмана.
 -
концентрация молекул у поверхности
Земли.
-
концентрация молекул у поверхности
Земли.
 -
концентрация молекул на высоте
-
концентрация молекул на высоте
 .
.
Теплоемкость.
Теплоемкостью тела называется физическая величина, равная отношению
 ,
,
 .
.
Теплоемкость одного моля – молярная теплоемкость
 .
.
Т.к.
 - функция процесса
- функция процесса ,
то
,
то .
.
Учитывая

 ;
;
 ;
;





 .
.
 -
формула Майера.
-
формула Майера.
Т.о.
задача вычисления теплоемкости сводится
к нахождению
 .
.
 .
.

Для
одного моля:

 ,
отсюда
,
отсюда .
.
Двухатомный газ (О 2 , N 2 , Cl 2 , СО и т.д.).
(модель жесткой гантели).
Полное число степеней свободы:
 .
.
Тогда
 ,
то
,
то
 ;
; .
.
Это значит, что теплоемкость должна быть постоянной. Вместе с тем опыт говорит, что теплоемкость зависит от температуры.
При понижении температуры "замараживаются" сначала колебательные степени свободы, а затем и вращательные степени свободы.
Согласно законам квантовой механики энергия гармонического осциллятора с классической частотой может принимать только дискретный набор значений
Многоатомные газы (H 2 O, CH 4 , C 4 H 10 O и т.д.).
 ;
;
 ;
; ;
;
 Сравним
теоретические данные с опытными.
Сравним
теоретические данные с опытными.
Видно,
что
 2-х атомных газов равняется
2-х атомных газов равняется ,
но изменяется при низких температурах
вопреки теории теплоемкости.
,
но изменяется при низких температурах
вопреки теории теплоемкости.
Такой
ход кривой
 от
от свидетельствует о «замораживании»
степеней свободы. Наоборот при больших
температурах подключаются дополнительные
степени свободы
эти данные ставят под сомнение теорему
о равномерном распределении. Современная
физика позволяет объяснить зависимость
свидетельствует о «замораживании»
степеней свободы. Наоборот при больших
температурах подключаются дополнительные
степени свободы
эти данные ставят под сомнение теорему
о равномерном распределении. Современная
физика позволяет объяснить зависимость
 от
от используя квантовые представления.
используя квантовые представления.
Квантовая
статистика устранила трудности в
объяснении зависимости теплоемкости
газов (в частности двухатомных газов)
от температуры. Согласно положениям
квантовой механики, энергия вращательного
движения молекул и энергия колебаний
атомов могут принимать лишь дискретные
значения. Если энергия теплового движения
значительно меньше разности энергий
соседних уровней энергии (),
то при столкновении молекул вращательные
и колебательные степени свободы
практически не возбуждаются. Поэтому
при низких температурах поведение
двухатомного газа подобно поведению
одноатомного.
Так как разность между
соседними вращательными уровнями
энергии значительно меньше, чем между
соседними колебательными уровнями (![]() ),
то с ростом температуры сначала
возбуждаются вращательные степени
свободы. В результате этого возрастает
теплоемкость. При дальнейшем увеличении
температуры возбуждаются и колебательные
степени свободы, и происходит дальнейший
рост теплоемкости.
А.
Эйнштейн, приближенно считал, что
колебания атомов кристаллической
решетки независимы. Используя модель
кристалла как совокупность независимо
колеблющихся с одинаковой частотой
гармонических осцилляторов, он создал
качественную квантовую теорию теплоемкости
кристаллической решетки. Эта теория
впоследствии была развита Дебаем,
который учел, что колебания атомов в
кристаллической решетке не являются
независимыми. Рассмотрев непрерывный
спектр частот осцилляторов, Дебай
показал, что основной вклад в среднюю
энергию квантового осциллятора вносят
колебания на низких частотах,
соответствующих упругим волнам.
Тепловое
возбуждение твердого тела можно описать
в виде упругих волн, распространяющихся
в кристалле. Согласно корпускулярно–волновому
дуализму свойств вещества, упругие
волны в кристалле сопоставляют
сквазичастицами–фононами
,
обладающими энергией .Фонон
– квант энергии упругой волны, являющийся
элементарным возбуждением, ведущим
себя подобно микрочастице.
Как
квантование электромагнитного излучения
привело к представлению о фотонах, так
квантование упругих волн (как результата
теплового колебания молекул твердых
тел) привело к представлению о фононах.
Энергия кристаллической решетки
складывается из энергии фононного газа.
Квазичастицы (в частности фононы) сильно
отличаются от обычных микрочастиц
(электронов, протонов, нейтронов и т.д.),
так как они связаны с коллективным
движением многих частиц системы.
),
то с ростом температуры сначала
возбуждаются вращательные степени
свободы. В результате этого возрастает
теплоемкость. При дальнейшем увеличении
температуры возбуждаются и колебательные
степени свободы, и происходит дальнейший
рост теплоемкости.
А.
Эйнштейн, приближенно считал, что
колебания атомов кристаллической
решетки независимы. Используя модель
кристалла как совокупность независимо
колеблющихся с одинаковой частотой
гармонических осцилляторов, он создал
качественную квантовую теорию теплоемкости
кристаллической решетки. Эта теория
впоследствии была развита Дебаем,
который учел, что колебания атомов в
кристаллической решетке не являются
независимыми. Рассмотрев непрерывный
спектр частот осцилляторов, Дебай
показал, что основной вклад в среднюю
энергию квантового осциллятора вносят
колебания на низких частотах,
соответствующих упругим волнам.
Тепловое
возбуждение твердого тела можно описать
в виде упругих волн, распространяющихся
в кристалле. Согласно корпускулярно–волновому
дуализму свойств вещества, упругие
волны в кристалле сопоставляют
сквазичастицами–фононами
,
обладающими энергией .Фонон
– квант энергии упругой волны, являющийся
элементарным возбуждением, ведущим
себя подобно микрочастице.
Как
квантование электромагнитного излучения
привело к представлению о фотонах, так
квантование упругих волн (как результата
теплового колебания молекул твердых
тел) привело к представлению о фононах.
Энергия кристаллической решетки
складывается из энергии фононного газа.
Квазичастицы (в частности фононы) сильно
отличаются от обычных микрочастиц
(электронов, протонов, нейтронов и т.д.),
так как они связаны с коллективным
движением многих частиц системы.
Фононы не могут возникать в вакууме, они существуют только в кристалле.
Импульс фонона обладает своеобразным свойством: при столкновении фононов в кристалле их импульс может дискретными порциями передаваться кристаллической решетке – импульс при этом не сохраняется. Поэтому в случае фононов говорят о квазиимпульсе.
Фононы имеют спин, равный нулю, и являются бозонами, а потому фононный газ подчиняется статистике Бозе–Эйнштейна.
Фононы могут испускаться и поглощаться, но их число не сохраняется постоянным.
Применение
статистики Бозе–Эйнштейна к фононному
газу (газу из независимых бозе–частиц)
привело Дебая к следующему
количественному выводу. При высоких
температурах, которые много больше
характеристической температуры
Дебая (классическая
область), теплоемкость твердых тел
описывается законом Дюлонга и Пти,
согласно которому молярная теплоемкость
химически простых тел в кристаллическом
состоянии одинакова ![]() и
не зависит от температуры.
При низких
температурах, когда (квантовая
область), теплоемкость пропорциональна
третьей степени термодинамической
температуры: Характеристическая
температура Дебая равна: ,
где –
предельная частота упругих колебаний
кристаллической решетки.
и
не зависит от температуры.
При низких
температурах, когда (квантовая
область), теплоемкость пропорциональна
третьей степени термодинамической
температуры: Характеристическая
температура Дебая равна: ,
где –
предельная частота упругих колебаний
кристаллической решетки.
Центральное понятие этой темы - понятие молекулы; сложность его усвоения школьниками связана с тем, что молекула - объект, непосредственно ненаблюдаемый. Поэтому учитель должен убедить десятиклассников в реальности микромира, в возможности его познания. В связи с этим большое внимание уделяют рассмотрению экспериментов, доказывающих существование и движение молекул и позволяющих вычислить их основные характеристики (классические опыты Перрена, Рэлея и Штерна). Кроме этого, целесообразно ознакомить учащихся с расчетными методами определения характеристик молекул. При рассмотрении доказательства существования и движения молекул рассказывают учащимся о наблюдениях Броуном беспорядочного движения мелких взвешенных частиц, которое не прекращалось в течение всего времени наблюдения. В то время не было дано правильного объяснения причины этого движения, и лишь спустя почти 80 лет А. Эйнштейн и М. Смолуховский построили, а Ж. Перрен экспериментально подтвердил теорию броуновского движения. Из рассмотрения опытов Броуна необходимо сделать следующие выводы: а) движение броуновских частиц вызывается ударами молекул вещества, в котором эти частицы взвешены; б) броуновское движение непрерывно и беспорядочно, оно зависит от свойств вещества, в котором частицы взвешены; в) движение броуновских частиц позволяет судить о движении молекул среды, в которой эти частицы находятся; г) броуновское движение доказывает существование молекул, их движение и непрерывный и хаотический характер этого движения. Подтверждение такого характера движения молекул было получено в опыте французского физика Дюнуайе (1911 г.), который показал, что молекулы газа движутся в различных направлениях и в отсутствие соударений их движение прямолинейно. В настоящее время факт существования молекул ни у кого не вызывает сомнения. Развитие техники позволило непосредственно наблюдать крупные молекулы. Рассказ о броуновском движении целесообразно сопровождать демонстрацией модели броуновского движения в вертикальной проекции с помощью проекционного фонаря или кодоскопа, а также показом кинофрагмента «Броуновское движение» из кинофильма «Молекулы и молекулярное движение». Кроме того, полезно провести наблюдение броуновского движения в жидкостях с помощью микроскопа. Препарат изготавливают из смеси равных частей двух растворов: 1%-ного раствора серной кислоты и 2%-ного водного раствора гипосульфита. В результате реакции образуются частицы серы, которые находятся в растворе во взвешенном состоянии. Две капли этой смеси помещают на предметное стекло и наблюдают за поведением частиц серы. Препарат можно изготовить из сильно разбавленного раствора молока в воде или из раствора акварельной краски в воде. При обсуждении вопроса о размерах молекул рассматривают сущность опыта Р. Рэлея, который заключается в следующем: на поверхность воды, налитой в большой сосуд, помещают каплю оливкового масла. Капля растекается по поверхности воды и образует круглую пленку. Рэлей предположил, что, когда капля перестает растекаться, ее толщина становится равной диаметру одной молекулы. Опыты показывают, что молекулы различных веществ имеют разные размеры, но для оценки размеров молекул принимают величину, равную 10 -10 м. В классе можно проделать аналогичный опыт. Для демонстрации расчетного метода определения размеров молекул приводят пример вычисления диаметров молекул различных веществ по их плотностям и постоянной Авогадро. Представить малые размеры молекул школьникам трудно, по этому полезно привести ряд примеров сравнительного характера. Например, если увеличить все размеры во столько раз, чтобы молекула была видна (т. е. до 0,1 мм), то песчинка превратилась бы в стометровую скалу, муравей увеличился бы до размеров океанского корабля, человек обладал бы ростом 1700 км. Число молекул в количестве вещества 1 моль можно определить по результатам опыта с мономолекулярным слоем. Зная диаметр молекулы, можно найти ее объем и объем количества вещества 1 моль, который равен где р - плотность жидкости. Отсюда определяют постоянную Авогадро. Расчетный метод заключается в определении числа молекул в количестве вещества 1 моль по известным значениям молярной массы и массы одной молекулы вещества. Значение постоянной Авогадро, по современным данным, 6,022169*10 23 моль -1 . С расчетным методом определения постоянной Авогадро можно ознакомить учащихся, предложив ее вычислить по значениям молярных масс разных веществ. Следует ознакомить школьников с числом Лошмидта, которое показывает, какое число молекул содержится в единице объема газа при нормальных условиях (оно равно 2,68799*10 -25 м -3). Десятиклассники могут самостоятельно определить число Лошмидта для нескольких газов и показать, что оно во всех случаях одно и то же. Приводя примеры, можно создать у ребят представление о том, насколько большим является число молекул в единице объема. Если в резиновом воздушном шаре сделать прокол настолько тонкий, что через него каждую секунду будет выходить по 1 000 000 молекул, то понадобится примерно 30 млрд. лет, чтобы все молекулы вышли. Один из методов определения массы молекул основан на опыте Перрена, который исходил из того, что капли смолы в воде ведут себя так же, как молекулы в атмосфере. Перрен подсчитывал число капелек в разных слоях эмульсии, выделив с помощью микроскопа слои толщиной 0,0001 см. Высота, на которой таких капелек в два раза меньше, чем у дна, была равна h = 3*10 -5 м. Масса одной капли смолы оказалась равной М = 8,5*10 -18 кг. Если бы наша атмосфера состояла только из молекул кислорода, то на высоте Н=5 км плотность кислорода была бы в два раза меньше, чем у поверхности Земли. Записывают пропорцию m/M=h/H, откуда находят массу молекулы кислорода m=5,1*10 -26 кг. Предлагают учащимся самостоятельно рассчитать массу молекулы водорода, плотность которого в два раза меньше, чем у поверхности Земли, на высоте H=80 км. В настоящее время значения масс молекул уточнены. Например, для кислорода установлено значение 5,31*10 -26 кг, а для водорода - 0,33*10 -26 кг. При обсуждении вопроса о скоростях движения молекул учащихся знакомят с классическим опытом Штерна. При объяснении опыта целесообразно создать его модель с помощью прибора «Вращающийся диск с принадлежностями». На краю диска в вертикальном положении укрепляют несколько спичек, в центре диска - трубку с желобом. Когда диск неподвижен, шарик, опущенный в трубку, скатываясь по желобу, сбивает одну из спичек. Затем диск приводят во вращение с определенной скоростью, зафиксированной по тахометру. Вновь пущенный шарик отклонится от первоначального направления движения (относительно диска) и собьет спичку, находящуюся на некотором расстоянии от первой. Зная это расстояние, радиус диска и скорость шарика на ободе диска, можно определить скорость движения шарика по радиусу. После этого целесообразно рассмотреть сущность опыта Штерна и конструкцию его установки, используя для иллюстрации кинофрагмент «Опыт Штерна». Обсуждая результаты опыта Штерна, обращают внимание на то, что существует определенное распределение молекул по скоростям, о чем свидетельствует наличие у полоски напыленных атомов определенной ширины, причем толщина этой, полоски различна. Кроме того, важно отметить, что молекулы, движущиеся с большой скоростью, оседают ближе к месту напротив щели. Наибольшее число молекул имеет наиболее вероятную скорость. Необходимо сообщить учащимся, что теоретически закон распределения молекул по скоростям был открыт Дж. К. Максвеллом. Распределение молекул по скоростям может быть промоделировано на доске Гальтона. Вопрос о взаимодействии молекул школьники уже изучали в VII классе, в X классе знания по этому вопросу углубляют и расширяют. Необходимо подчеркнуть следующие моменты: а) межмолекулярное взаимодействие имеет электромагнитную природу; б) межмолекулярное взаимодействие характеризуется силами притяжения и отталкивания; в) силы межмолекулярного взаимодействия действуют на расстояниях, не больших 2-3 диаметров молекул, причем на этом расстоянии заметна лишь сила притяжения, силы отталкивания практически равны нулю; г) по мере уменьшения расстояния между молекулами силы взаимодействия увеличиваются, причем сила отталкивания растет быстрее (пропорционально г -9), чем сила притяжения (пропорционально r -7 ). Поэтому при уменьшении расстояния между молекулами сначала преобладает сила притяжения, затем при некотором расстоянии r о сила притяжения равна силе отталкивания и при дальнейшем сближении преобладает сила отталкивания. Все вышесказанное целесообразно проиллюстрировать графиком зависимости от расстояния сначала силы притяжения, силы отталкивания, а затем равнодействующей силы. Полезно построить график потенциальной энергии взаимодействия, который в дальнейшем можно использовать при рассмотрении агрегатных состояний вещества. Внимание десятиклассников обращают на то, что состоянию устойчивого равновесия взаимодействующих частиц соответствует равенство нулю равнодействующей сил взаимодействия и наименьшее значение их взаимной потенциальной энергии. В твердом теле энергия взаимодействия частиц (энергия связи) много больше кинетической энергии их теплового движения, поэтому движение частиц твердого тела представляет собой колебания относительно узлов кристаллической решетки. Если кинетическая энергия теплового движения молекул много больше потенциальной энергии их взаимодействия, то движение молекул полностью беспорядочное и вещество существует в газообразном состоянии. Если кинетическая энергия теплового движения частиц сравнима с потенциальной энергией их взаимодействия, то вещество находится в жидком состоянии.
Согласно молекулярно-кинетической теории все вещества состоят из мельчайших частиц - молекул. Молекулы разделены промежутками, находятся в непрерывном движении и взаимодействуют между собой. Молекула - наименьшая частица вещества, обладающая его химическими свойствами. Молекулы состоят из более простых частиц - атомов химических элементов. Молекулы различных веществ имеют различный атомный состав.
Молекулы обладают кинетической энергией и одновременно потенциальной энергией взаимодействия. В газообразном состоянии W кин >> W пот. В жидком и твердом состояниях кинетическая энергия частиц сравнима с энергией их взаимодействия (W кин ~W пот).
Поясним три основных положения молекулярно - кинетической теории.
1. Все вещества состоят из молекул, т.е. имеют дискретное строение, молекулы разделены промежутками.
2. Молекулы находятся в непрерывном беспорядочном (хаотическом) движении.
3. Между молекулами тела существуют силы взаимодействия.
Молекулярно-кинетическая теория обосновывается многочисленными опытами и огромным количеством физических явлений.
Наличие промежутков между молекулами следует, например, из опытов смешения различных жидкостей: объем смеси всегда меньше суммы объемов смешанных жидкостей.
Приведем некоторые из доказательств беспорядочного (хаотического) движения молекул:
а) стремление газа занять весь предоставленный ему объем (распространение пахучего газа по всему помещению);
б) броуновское движение - беспорядочное движение мельчайших видимых в микроскоп частиц вещества, находящихся во взвешенном состоянии и нерастворимых в ней. Это движение происходит под действием беспорядочных ударов молекул, окружающей жидкости, находящихся в постоянном хаотическом движении;
в) диффузия - взаимное проникновение молекул соприкасающихся веществ. При диффузии молекулы одного тела, находясь в непрерывном движении, проникают в промежутки между молекулами другого соприкасающегося с ним тела и распространяются между ними. Диффузия проявляется во всех телах - в газах, жидкостях и твердых телах, - но в разной степени.
Диффузию в газах можно наблюдать, если сосуд с пахучим газом открыть в помещении. Через некоторое время газ распространится по всему помещению.
Диффузия в жидкостях происходит значительно медленнее, чем в газах. Например, в стакан нальем раствор медного купороса, а затем, очень осторожно добавим слой воды и оставим стакан в помещении с постоянной температурой, и где он не подвергается сотрясениям. Через некоторое время будем наблюдать исчезновение резкой границы между купоросом и водой, а через несколько дней жидкости перемешаются, несмотря на то, что плотность купороса больше плотности воды. Так же диффундирует вода со спиртом и прочие жидкости.
Диффузия в твердых телах происходит еще медленнее, чем в жидкостях (от нескольких часов до нескольких лет). Она может наблюдаться только в хорошо пришлифованных телах, когда расстояния между поверхностями пришлифованных тел близки к расстояниям между молекулами (10 -8 см). При этом скорость диффузии увеличивается при повышении температуры и давления.
Доказательства силового взаимодействия молекул:
а) деформация тел под влиянием силового воздействия;
б) сохранение формы твердыми телами;
в) поверхностное натяжение жидкостей и, как следствие, явление смачивания и капиллярности.
Между молекулами существуют одновременно силы притяжения и силы отталкивания. Эти силы имеют электромагнитную природу.
Рассмотрим различные случаи взаиморасположения молекул и покажем какие силы преобладают. Введем следующие обозначения:
r – Расстояние между молекулами.
d – диаметр молекулы
F np – сила притяжения
F om – сила отталкивания
→ - стремиться
Следовательно
r→∞ => F=0 (силы короткодействующие)
r > d (≈2-3 диаметра)=> F np > F om
r→d=>F np →0
Данный видеоурок посвящен теме «Основные положения МКТ. Строение вещества. Молекула». Здесь вы узнаете, что изучает молекулярно-кинетическая теория (МКТ) в физике. Познакомитесь с тремя основными положениями, на которых базируется МКТ. Узнаете, чем определяются физические свойства вещества и что представляют собой атом и молекула.
Для начала давайте вспомним все предыдущие разделы физики, которые мы изучали, и поймём, что всё это время мы рассматривали процессы, происходящие с макроскопическими телами (или объектами макромира). Теперь же мы будем изучать их строение и процессы, протекающие внутри них.
Определение. Макроскопическое тело - тело, состоящее из большого числа частиц. Например: машина, человек, планета, бильярдный шар…
Микроскопическое тело - тело, состоящее из одной или нескольких частиц. Например: атом, молекула, электрон… (рис. 1)

Рис. 1. Примеры микро- и макрообъектов соответственно
Определив таким образом предмет изучения курса МКТ, следует теперь поговорить об основных целях, которые ставит перед собой курс МКТ, а именно:
- Изучение процессов, происходящих внутри макроскопического тела (движение и взаимодействие частиц)
- Свойства тел (плотность, масса, давление (для газов)…)
- Изучение тепловых явлений (нагревание-охлаждение, изменения агрегатных состояний тела)
Изучение этих вопросов, которое будет проходить на протяжении всей темы, начнётся сейчас с того, что мы сформулируем так называемые основные положения МКТ, то есть некоторые утверждения, истинность которых уже давно не подвергается сомнениям, и, отталкиваясь от которых, будет строиться весь дальнейший курс.
Разберём их по очереди:
Все вещества состоят из большого количества частиц - молекул и атомов.
Определение. Атом - мельчайшая частица химического элемента. Размеры атомов (их диаметр) имеет порядок см. Стоит отметить, что различных типов атомов, в отличие от молекул, относительно немного. Все их разновидности, которые на сегодняшний день известны человеку, собраны в так называемой таблице Менделеева (см. рис. 2)

Рис. 2. Периодическая таблица химических элементов (по сути разновидностей атомов) Д. И. Менделеева
Молекула - структурная единица вещества, состоящая из атомов. В отличие от атомов, они больше и тяжелее последних, а главное, они обладают огромным разнообразием.
Вещество, молекулы которого состоят из одного атома, называются атомарными , из большего количества - молекулярными . Например: кислород, вода, поваренная соль () - молекулярные; гелий серебро (He, Ag) - атомарные.
Причём следует понимать, что свойства макроскопических тел будут зависеть не только от количественной характеристики их микроскопического состава, но и от качественной.

Если в строении атомов вещество имеет какую-то определённую геометрию (кристаллическую решётку ), или же, наоборот, не имеет, то этим телам будут присущи различные свойства. Например, аморфные тела не имеют строгой температуры плавления. Самый известный пример - это аморфный графит и кристаллический алмаз. Оба вещества состоят из атомов углерода.


Рис. 3. Графит и алмаз соответственно
Таким образом «из скольких, в каком взаимном расположении и каких атомов и молекул состоит вещество?» - первый вопрос, ответ на который приблизит нас к пониманию свойств тел.
Все упомянутые выше частицы находятся в непрерывном тепловом хаотическом движении.
Так же, как и в рассматриваемых выше примерах, важно понимание не только количественных аспектов этого движения, но и качественных для различных веществ.
Молекулы и атомы твёрдых тел совершают лишь небольшие колебания относительно своего постоянного положения; жидких - также совершают колебания, но из-за больших размеров межмолекулярного пространства иногда меняются местами друг с другом; частички газа, в свою очередь, практически не сталкиваясь, свободно перемещаются в пространстве.
Частицы взаимодействуют друг с другом.
Взаимодействие это носит электромагнитный характер (взаимодействия ядер и электронов атома) и действует в обе стороны (как притягивание, так и отталкивание).

Здесь: d - расстояние между частицами; a - размеры частиц (диаметр).
Впервые понятие «атом» было введено древнегреческим философом и естествоведом Демокритом (рис. 4). В более поздний период активно задался вопросом о структуре микромира русский учёный Ломоносов (рис. 5).

Рис. 4. Демокрит

Рис. 5. Ломоносов
На следующем занятии мы введём методы качественного обоснования основным положениям МКТ.
Список литературы
- Мякишев Г.Я., Синяков А.З. Молекулярная физика. Термодинамика. - М.: Дрофа, 2010.
- Генденштейн Л.Э., Дик Ю.И. Физика 10 класс. - М.: Илекса, 2005.
- Касьянов В.А. Физика 10 класс. - М.: Дрофа, 2010.
- Elementy.ru ().
- Samlib.ru ().
- Youtube ().
Домашнее задание
- *Благодаря какой силе возможно сделать эксперимент по измерению размеров молекулы масла, показанный в видеоуроке?
- Почему молекулярно-кинетическая теория не рассматривает органические соединения?
- Почему даже очень маленькая песчинка песка является объектом макромира?
- Силы преимущественно какой природы действуют на частицы со стороны других частиц?
- Как определить, является ли некая химическая структура химическим элементом?
Нас окружают разнообразные предметы. Мы можем увидеть, что это либо твердые тела, либо жидкости, либо газы. Возникает масса вопросов обо всем, что нас окружает. Ответы на многие вопросы дает молекулярно-кинетическая теория .
Молекулярно-кинетическая теория – это совокупность воззрений, используемых для описания наблюдаемых и измеряемых свойств вещества на основе изучения свойств атомов и молекул данного вещества, их взаимодействия и движения.
Основные положения молекулярно-кинетической теории
Все тела состоят из частиц – атомов, молекул, ионов.
Все частицы находятся в непрерывном хаотическом тепловом движении.
Между частицами любого тела существуют силы взаимодействия – притяжения и отталкивания.
Таким образом, в молекулярно-кинетической теории объектом исследования является система, состоящая из большого количества частиц – макросистема . Для объяснения поведения такой системы законы механики не применимы. Поэтому основным методом исследования является статистический метод изучения свойств вещества.
Для объяснения и предсказания явлений важно знать основные характеристики молекул :
- Размеры

Оценка размера молекулы может быть сделана как размер кубика a в котором содержится одна молекула, исходя из плотности твердых или жидких веществ и массы одной молекулы:

- Масса молекул
Отношение массы вещества m к числу молекул N в данном веществе:
- Относительная молекулярная масса
Отношение массы молекулы (или атома) данного вещества к 1/12 массы атома углерода:
- Количество вещества
Количество вещества равно отношению числа частиц N в теле (атомов – в атомарном веществе, молекул – в молекулярном) к числу молекул в одном моле веществаN А:

- Постоянная Авогадро
Количество молекул, содержащихся в 1 моль вещества.
- Молярная масса
Молярной массой вещества называют массу вещества, взятого в количестве 1 моля.
В Международной системе единиц молярная масса вещества выражается в кг/моль .
- Взаимодействие (количественно на основе опытов)
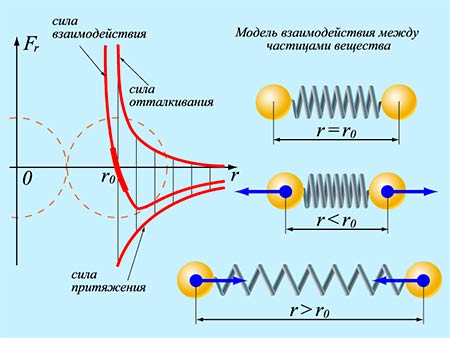
Для взаимодействия молекул характерно одновременно и притяжение, и отталкивание: на расстояниях r
Молекулярно-кинетическая теория дает возможность понять, почему вещество может находиться в газообразном, жидком и твердом состояниях. С точки зрения МКТ агрегатные состояния различаются по значению среднего расстояния между молекулами и характеру движения молекул друг относительно друга .
Основные положения молекулярно-кинетической теории неоднократно подтверждались различными физическими экспериментами. Например, исследованием:
А) Диффузии
Б) Броуновского движения
Краткие итоги
Молекулярно-кинетическая теория объясняет строение и свойства тел на основе движения и взаимодействия атомов, молекул и ионов. В основе МКТ лежат три положения , которые полностью подтверждены экспериментально и теоретически:
1) все тела состоят из частиц – молекул, атомов, ионов;
2) частицы находятся в непрерывном хаотическом тепловом движении;
3) между частицами любого тела существуют силы взаимодействия – притяжения и отталкивания.
Молекулярное строение вещества подтверждается непосредственным наблюдением молекул в электронных микроскопах, а также растворением твердых веществ в жидкостях, сжимаемостью и проницаемостью вещества. Тепловое движение – броуновским движением и диффузией. Наличие межмолекулярного взаимодействия прочностью и упругостью твердых тел, поверхностным натяжением жидкостей.
Опорный конспект к уроку:

Вопросы для самоконтроля по блоку «Основные положения молекулярно-кинетической теории и их опытное обоснование»
- Сформулируйте основные положения молекулярно-кинетической теории.
- Какие наблюдения и эксперименты подтверждают основные положения молекулярно-кинетической теории?
- Что такое молекула? атом?
- Что называют относительной молекулярной массой? Какая формула выражает это понятие?
- Что называют количеством вещества? Какая формула выражает это понятие? Какова единица количества вещества?
- Что называют постоянной Авогадро?
- Что такое молярная масса вещества? Какая формула выражает смысл этого понятия? Какова единица молярной массы?
- Какова природа межмолекулярных сил?
- Какими свойствами обладают силы молекулярного взаимодействия?
- Как силы взаимодействия зависят от расстояния между ними?
- Опишите характер движения молекул в газах, жидкостях и твердых телах.
- Каков характер упаковки частиц у газов, жидкостей и твердых тел?
- Каково среднее расстояние между молекулами у газов, жидкостей и твердых тел?
- Перечислите основные свойства газов, жидкостей, твердых тел.
- Что называют броуновским движением?
- О чем свидетельствует броуновское движение?
- Что называют диффузией? Приведите примеры диффузии в газах, жидкостях и твердых телах.
- 18. Как зависит скорость диффузии от температуры тел?
 Рис.
3.3
Рис.
3.3